Fillarina LIFT Monofásico Ácido Hialurónico Relleno Dermal con Lidocaína
Nome: FILLARINA LIFT
Atributo: Relleno inxectábel de ácido hialurónico monofásico reticulado con lidocaína
Concentración de HA: 22mg / ml
Buffer de fosfato pH 7,2 : q.s.
Lidocaína: 3mg/ml
- Vista xeral
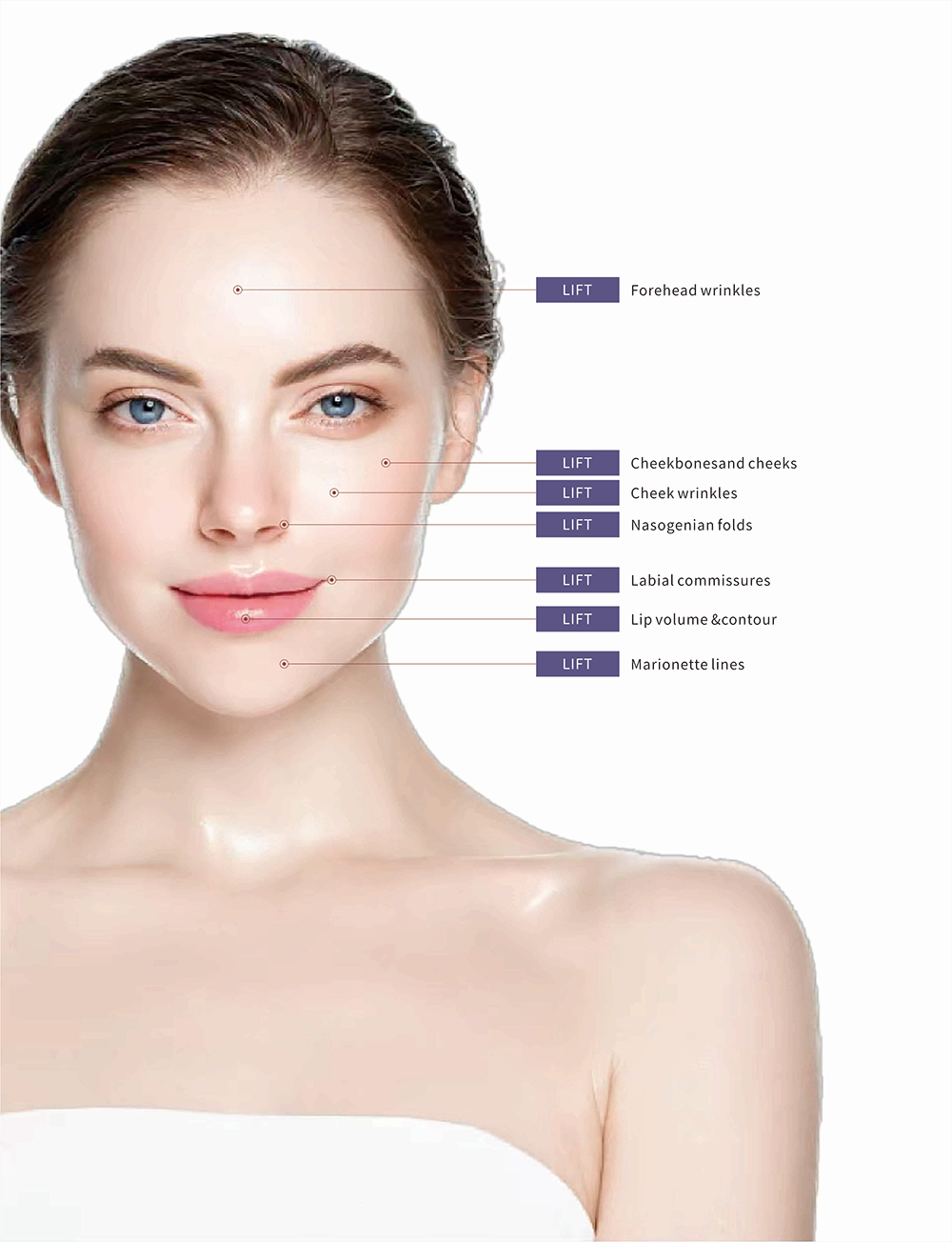
Os rellenos dérmicos Fillarina LIFT úsanse para a corrección de liñas finas e arrugas ou defectos faciais.
FILLARINA de Tiera Biotechnology é unha nova liña de 3 recheos monofásicos de ácido hialurónico utilizados para mellorar a miniaturización da pel, corrixir arrugas superficiais a profundas, aumentar o volume, definir áreas faciais e apertar os poros. FILLARINA é un recheo monofásico de ácido hialurónico que inclúe lidocaína e combina tamaños máis pequenos de partículas cunha eficacia duradeira. Cada presentación consiste nunha alta concentración de ácido hialurónico e substancias naturais utilizadas para fornecer á pel os nutrientes necesarios, volume e hidratación.
| Nome | FILLARINA LIFT |
| Atributo | Relleno inxectábel de ácido hialurónico monofásico reticulado con lidocaína |
| Concentración de HA | 22mg / ml |
| Buffer de fosfato pH 7,2 | q.s. |
| Lidocaína | 3mg/ml |
| Condición de almacenamento | Mantén a temperatura entre 2 °C e 25 °C, non congeles. |
| Indicacións para o uso | FlLLARlNA xel inxectábel está indicado para a inxección na dermis media a profunda para a corrección de depresións medias e/ou profundas da pelle, así como para a definición e realce dos lábios. |
Contraindicacións
•FlLLARINA está contraindicado para pacientes con alergias graves manifestadas por un historial de anafilaxia ou historial ou presenza de múltiples alergias graves.
•FlLLARINA contén cantidades traza de proteínas bacterianas gram-positivas e está contraindicado para pacientes con historial de alergias a este material.
•FlLLARlNA contén cantidades traza de lidocaína e está contraindicado para pacientes con historial de alergias a este material.
PRECAUCIÓNS PARA O USO
•FILLARINA é embalada para uso de un só paciente. Non readecstrar. Non a utilice se a embalaxe está aberta ou danada. FILLARINA só está indicada para inxeccións intra-dermais e inxeccións na membrana mucosa dos labios. Baseado en estudos preclínicos, os pacientes deben estar limitados a 20 mL de FILLARINA por 60 kg (130 lbs) de masa corporal por ano. A seguridade de inxectar cantidades mellores non foi establecida. A seguridade e eficacia no tratamento de rexións anatômicas distintas das arrugas e pliegues faciais (p.ex., labios) non foron establecidas en estudos clínicos controlados. Como en todas as procedementos transcutáneos, a implantación de recheo dérmico porta un risco de infección. Deben seguirse as precaucións estándar asociadas coas substancias inxectables. * FILLARINA debe ser usada tal como se fornece. A modificación ou uso do produto fóra das Instrucións de Uso pode afectar adversamente á esterilidade, homoxeneidade e rendemento do produto, polo que xa non podería asegurarse.
•A seguridade para o uso durante a gravidez, no aleitamento materno ou en pacientes con menos de 18 anos non foi estabelecida.
•A seguridade en pacientes coa susceptibilidade coñecida á formación de queloide, cicatrices hipertróficas e trastornos de pigmentación non foi estudada.
•FILLARINA debe usarse con precaución en pacientes que reciben terapia inmunossupresora.
•Os pacientes que toman sustancias que poden prolongar a sangría (como a aspirina, os medicamentos antiinflamatorios non esteroideos e a varfarina) poden, como calquera inxectión, experimentar un aumento das moreas ou da sangría nos lugares de inxección.
• Despois do uso, as seringas e agulhas de tratamento poden ser potenciais biohazards. Maneixe e desarte dese items de acordo coa práctica médica aceptada e cos requisitos locais, estatais e federais aplicables.
•O xel injectable FILLARINA é un xel claro e incolor sen partículas. No caso de que o contido dunha seringa mostre signos de separación e/ou pare nublado, non use a seringa; notifique ao Soporte de Produtos Sinclean ao +86-519-85855985.
•se se considera un tratamento con laser, peelado químico ou calquera outro procedemento baseado nunha resposta dérmica activa despois do tratamento co FILLARINA, existe un risco posible de provocar unha reacción inflamatoria no lugar das indicacións. Tamén é posible unha reacción inflamatoria se o produto se administra antes de que a pelle se curase completamente despois dun tal procedemento.
•O incumprimento das instrucións para a conexión da agulla podería provocar a desconexión da agulla e/ou a fuga do produto na conexión entre o luerlock e o cabezal da agulla. Se a agulla está bloqueda, non aumente a presión no varetón, senón detña a inxección e cambie a agulla. Os atletas deben ser informados de que este produto contén un principio activo que pode dar un resultado positivo nun test antidoping. Os profesionais médicos deben ter en conta que este produto contén lidocaína. A composición deste produto é compatible cos campos utilizados para a imaxe por resonancia magnética.
EFECTOS SECUNDARIOS
•Os pacientes deben ser informados de que existen efectos secundarios potenciais asociados coa implantación deste produto, que poden ocorrer inmediatamente ou con atraso. Estes inclúen, pero non se limitan a: Reaccións inflamatorias (vermellura, edema, eritema, etc., que poden estar asociadas con picazón ou dor ao tacto ou ambas, que ocorren despois da inxección. Estas reaccións poden durar unha semana. Hematomas. Induración ou nódulos no lugar da inxección. Manchas ou descoloración do lugar da inxección.
•Efecto pobre ou débil efecto de enchimento.
•Houbo informes de casos de necroses na rexión glabellar, abcesos, granuloma e hipersensibilidade inmediata ou demorada despois das inxeccións de ácido hialurónico. Por iso, é aconsexable ter en conta estes riscos potenciais.
•Os pacientes deben informar á súa práctica médica tan pronto como sexa posible sobre as reaccións inflamatorias que persistan máis dunha semana ou calquera outro efecto secundario que desenvolva. A práctica médica debe empregar un tratamento apropiado.
•Calquera outro efecto secundario indexado asociado coa inxección de FILLARINA debe comunicarse ao distribuidor e/ou ao fabricante.