Fillarina LIFT Monophasisk Hyaluronsyrlige Dermal Filler med Lidokain
Navn: FILLARINA LIFT
Attributt: Krysslinket monofasisk hyaluronsyrlig injeksjonsfyller med lidokain
HA-konsentrasjon: 22mg / ml
Fosfatpuffert pH 7.2 : q.s.
Lidokain: 3mg/ml
- Oversikt
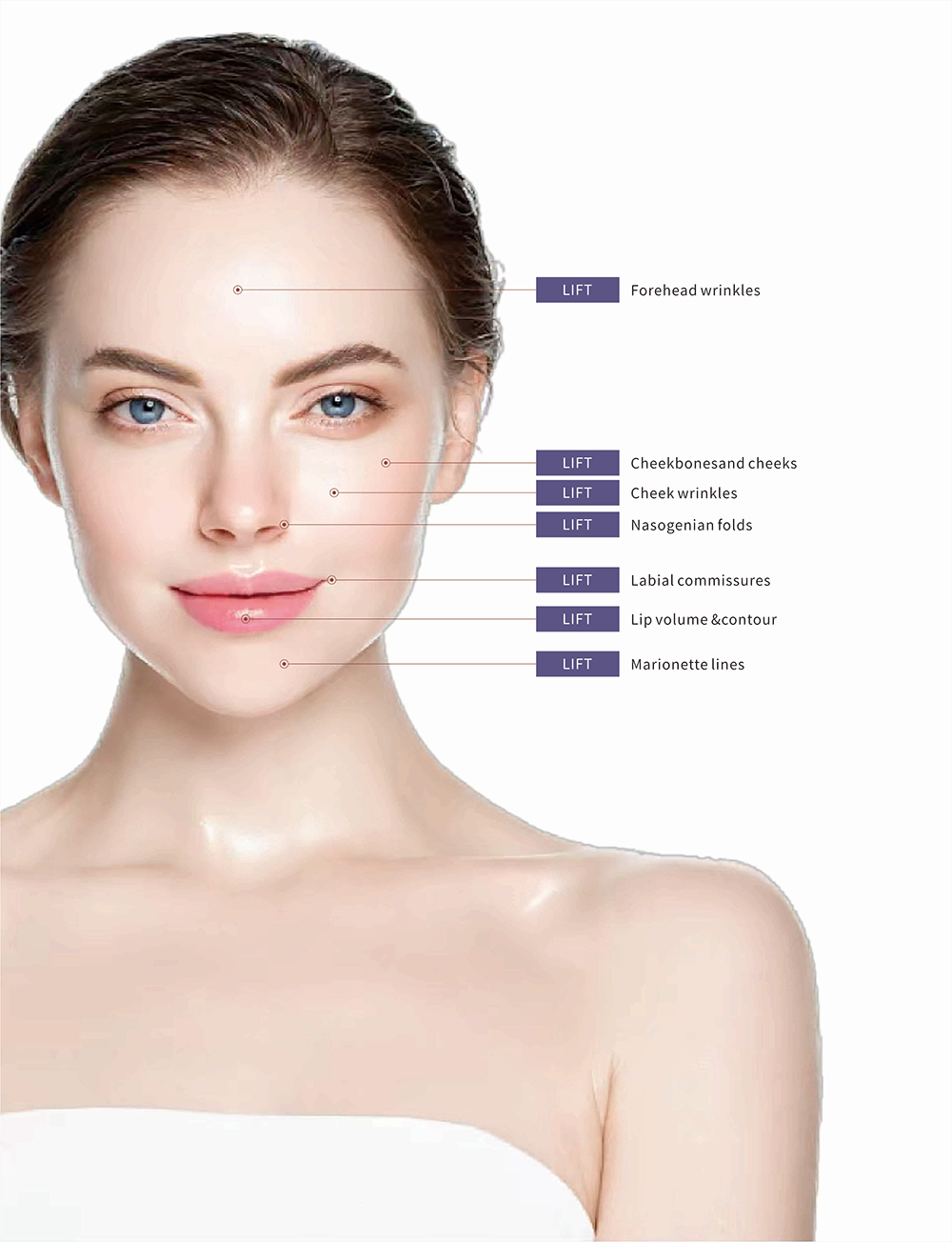
Fillarina LIFT dermal fyllere brukes til korreksjon av fine linjer og rynker eller ansiktets defekter.
FILLARINA fra Tiera Biotechnology er en ny serie med 3 monofasige hyaluronsyre-fyllere som brukes til å forbedre hudminiatyrisering, korrigere overfladiske til dybe rynker, øke volum, modellere ansiktsområder og stramme porer. FILLARINA er en monofasisk hyaluronsyre-fyller som inneholder lidokain, og som kombinerer små partikkler med langvarig effekt. Hver fyller består av en høy konsentrasjon av hyaluronsyre og naturlige stoffer som brukes til å gi huden nødvendige næringsstoffer, volum og hudfuktighet.
| Navn | FILLARINA LIFT |
| Attributt | Krysslinket monofasisk hyaluronsyrlig injeksjonsfyller med lidokain |
| HA-konsentrasjon | 22mg / ml |
| Fosfatpuffert pH 7.2 | q.s. |
| Lidokain | 3mg/ml |
| Oppbevaringsbetingelse | Lagre mellom 2 °C og 25 °C, frys ikke. |
| Indikasjoner for bruk | FlLLARlNA injekterbart gelfyller er indikert for injeksjon i mellom- til dype lager av den dermale for å korrigere mellom- og/eller dypt depresjoner i huden, samt for definisjon og forbedring av lepper. |
Kontraindikasjoner
•FlLLARINA er kontraindikert for pasienter med alvorlige allergier manifestert ved en historie av anafylakse eller historie eller tilstedeværelse av flere alvorlige allergier.
•FlLLARINA inneholder spore av gram-positiv bakteriel protein og er kontraindikert for pasienter med en historie av allergi mot slikt materiale.
•FlLLARlNA inneholder spore av lidokain og er kontraindikert for pasienter med en historie av allergi mot slikt materiale.
Forholdsregler for bruk
•FILLARINA er pakket for enkelt-pasient-bruk. Steriliser ikke på nytt. Bruk ikke hvis emballagen er åpen eller skadet. FILLARINA er kun indikert for intradermale injeksjoner og injeksjoner i leppenes slemhinn. Basert på prekliniske studier bør pasienter begrenses til 20 mL FILLARINA per 60 kg (130 lbs) kroppsmasse per år. Sikkerheten ved å injisere større mengder har ikke blitt etablert. Sikkerheten og effektiviteten ved behandling av anatomiområder andre enn fjesonsriner og -furer (f.eks. lepper) har ikke blitt etablert i kontrollerte kliniske studier. Som med alle transkutane prosedyrer, bærer dermal fylleimplantering risiko for infeksjon. Standardforholdsreglene knyttet til injiserbare materialer bør følges. FILLARINA skal brukes slik den leveres. Endring av produktet eller bruk utenfor Bruksanvisningen kan negativt påvirke steriliteten, homogeniteten og ytelsen til produktet, og det kan derfor ikke lenger garanteres.
•Sikkerheten for bruk under svangerskap, ved amming eller hos pasienter under 18 år er ikke etablert.
•Sikkerheten for pasienter med kjent oppfatning av keloidebildning, hypertrofisk armering og fargestørrelser har ikke blitt studert.
•FILLARINA bør brukes med forsiktighet hos pasienter på immunundertrykkende terapi.
•Pasienter som bruker stoffer som kan forlenge blødning (som aspirin, ikke-steroidiske motfeilingsmidler og warfarin) kan, som med enhver injeksjon, oppleve økt blåmærke eller blødning på injeksjonssteder.
• Etter bruk kan behandlingsnål og -syringer være potensielle biofarestoff. Behandle og fjern disse elementene i overensstemmelse med aksepterte medisinske praksiser og gjeldende lokale, statlige og federale krav.
•FILLARINA injeksjonsjel er en klar, fargetri jell uten partikler. Hvis innholdet i en syringe viser tegn på separasjon og/eller ser skygg ut, bruk ikke syringen; varsle Sinclean Produktstøtte på +86-519-85855985.
•hvis laserbehandling, kemisk peelings eller andre prosedyrer basert på aktiv dermal respons overveies etter behandling med FILLARINA, finnes det en mulig risiko for å utløse en inflammasjonsreaksjon på indikasjonsområdet. En inflammasjonsreaksjon er også mulig hvis produktet blir gitt før huden har helmet fullstendig etter slik en prosedyre.
•Manglende oppfyllelse av instruksjonene for klingenopphengning kan føre til at klingen løsner og/eller at produktet lekkjer ved luer-lock og klinehub-forbindelsen. Hvis klingen er blokkert, økkes ikke trykket på plungerstaven, men stopp injeksjonen og bytt klingen. Idrettsutøvere bør informeres om at dette produktet inneholder et virkestoff som kan gi en positiv reaksjon i antidopingtest. Medisinske praksitioner må ta hensyn til at dette produktet inneholder lidokain. Sammensetningen av dette produktet er kompatibel med felt brukt for magnetresonansbilde.
BIVIRKNINGER
•Pasientene må informeres om at det finnes potensielle bivirkninger knyttet til implantasjon av dette produktet, som kan oppstå umiddelbart eller være forsinkede. Disse inkluderer, men er ikke begrenset til: Inflammatoriske reaksjoner (rødhet, hevelse, erytem, etc., som kan være knyttet til kløe eller smerte ved trykk eller begge deler, som oppstår etter injeksjon. Slike reaksjoner kan vare i en uke. Blåmerker. Forhardning eller knuter på injeksjonsstedet. Flekker eller misfarging av injeksjonsstedet.
•Dårlig effekt eller svak fyllings-effekt.
•Tilfeller med narkose i glabellarområdet, abcesser, granulomat og umiddelbar eller utsatt hypersensitivitet etter hyaluronsyreinjeksjoner har blitt rapportert. Det er derfor rådgivende å ta hensyn til disse potensielle risikoenes.
•Pasientene må melde inflammatory reaksjoner som varer lenger enn en uke, eller noen andre bivirkninger som utvikler seg, til sin lege så fort som mulig. Den medisinske praksjoneren bør bruke en passende behandling.
•Eventuelle andre uønskede bivirkninger forbundet med injeksjon av FILLARINA må rapporteres til distributøren og/eller til fabrikanten.