Dermeca Plla Fyller 1 ml, Kollagenstimulator
Navn: Dermeca Lido Injectable Plla Fyller
Attributt: Injecterbart ansiktimplantat
PLLA-b-PEG mikrosfærer : 150mg/ml
HA-konsentrasjon: 17mg/ml
Lidokain : 0.3mg/ml
- Oversikt
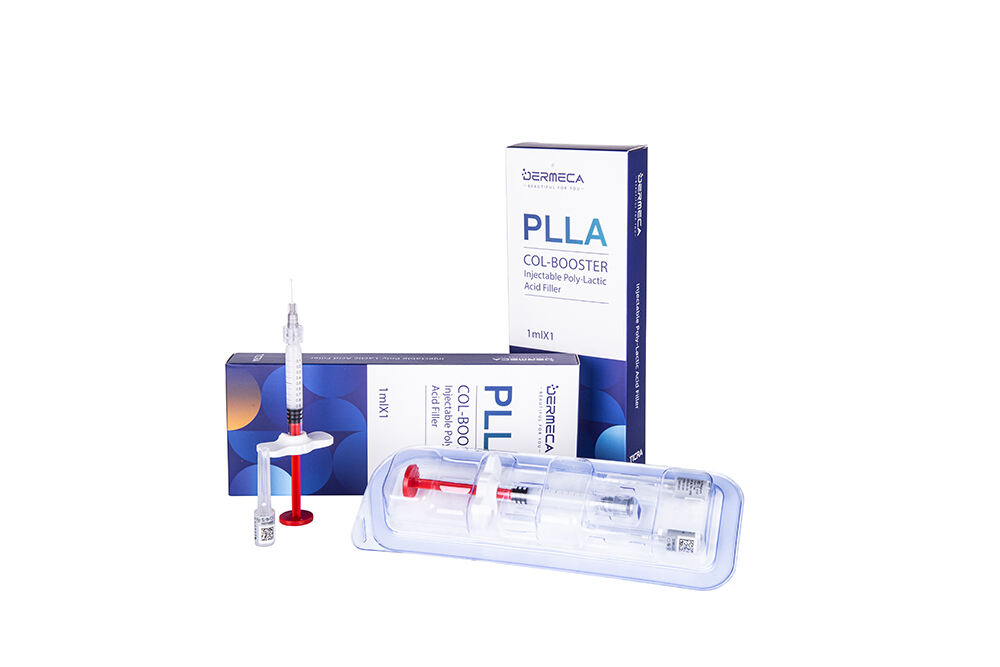
Dermeca Plla Filler, en formulering av tverrbundet natriumhyaluronatgel infundert med PLLA-mikrosfærer, er nøye utviklet for målrettede injeksjoner i områder som trenger volumøkning og løftingseffekter. Den er ideell for ansiktssoner som tinningene, brynerekken, nesestrukturen, columella nasi, hakeområdet, nesets grunnflate og dypt liggende kindmuskulatur, og gir en subtil og ungdommeliggjørende effekt. Behandlingen er utviklet for å gi et resultat som både virker naturlig og gjenoppretter ungdomsfulle konturer.
Dermeca Plla Filler består av en forhåndsutfylt sprøyte, en steril hypodermisk nål til engangsbruk, og gelen som er forhåndsutfylt i sprøyten. Gelen er hovedsaklig sammensatt av krysslenket natriumhyaluronat, poly-l-laktinsyrsamikrosfærer (PLLA) (merknadsverd innhold: 18 %), lidokainhydroklorid, og fosfatbuffersystemet. De nominelle konsentrasjonene av natriumhyaluronat (beredt ved mikrobiell ferming) og lidokainhydroklorid er henholdsvis 17 mg/mL og 3 mg/mL. Sprøyten med den forhåndsutfylte gelen er sterilisert ved dampsterilisering, og den sterile hypodermiske nålen til engangsbruk er sterilisert ved etylenoxid eller stråling. Fylleren er til engangsbruk (lagringslivstid: 2 år).
Fylleren er en melkete hvite, tykk gel med krysslinket natriumhyaluronat og PLLA-mikrosfærer som hovedbestanddeler. Den mediane partikkelstørrelsen på PLLA-mikrosfærer er 32 μm ± 6 μm, derav mer enn 95 % av mikrosfærerne har størrelse på 20–45 μm. Gellen er en hudvævsfyller som injiseres i de dype lagene av den dermale og subkutane overflate- og dypelagene for å korrigere nasolabiale folder, og PLLA-mikrosfærerne i gellen kan forlengre fyllingsvarigheten. Wrinkle Severity Rating Scale (WSRS)-poengsummen er fortsatt over 1 poeng etter 12 måneder hos de fleste subjekter som viste forbedring.
| Navn | Dermeca Lido Injectable Plla Fyller |
| Attributt | Injecterbart ansiktimplantat |
| HA-konsentrasjon | 17mg/ml |
| PLLA-b-PEG mikrosfære | 150mg/ml |
| Lidokain | 0.3mg/ml |
| Versjon | Lidokain |
| Injeksjonsone | Ansikt |
| Varighetsperiode for effekt | Opp til 2 år |
| Oppbevaringsbetingelse | Lagres mellom 2°C–25°C, og ikke fryses |
| Indikasjoner for bruk | Gellen er indikert for injeksjon i de dypte lagene av den dermale og subkutane overflate- og dypelagene for å korrigere moderat til alvorlige nasolabiale folder. |
Kontraindikasjoner
•Tidlig innsetting eller aktiv autoimmune sykdommer, under behandling med immunsuppressive eller immunnodulerende midler, aktiv hudinfeksjon.
•Herpes.
•Allergi mot hyaluronsyre, poly-l-laktisk syre, mælkesyre, polyetylenglykol eller lidokain (lokalanestetikum).
•Forstyrrelser i koagulasjonsmekanismer; behandlet med trombusoppløsende midler, antikoagulantia eller platekoagulasjonsinhibitorer de siste to ukene før injeksjon.
•Gravide/ammande kvinner og mindreårige.
•Keloid/hypertrof arrskonstitusjon.
Advarsel
•Før produktet brukes, må leger nøye lese bruksanvisningen for å forstå produktets egenskaper og relaterte injeksjonsrisikoer. Legene skal gi pasienten rådgivning og drøfte potensielle fordeler og risikoer ved behandlingen.
• Selve injeksjonsterapiproceduren medfører en risiko for infeksjon. Derfor bør rutinemessige tiltak knyttet til injeksjonsterapi følges. Før injeksjonen bør lokal desinfeksjon utføres; under injeksjonen må de sterile driftsreglene for kirurgisk behandling strengt overholdes.
•For pasienter som tar medisiner som påvirker blodplatefunksjonen, kan injeksjon føre til blåmerker eller blødning ved injeksjonsstedet.
•Gelens effekt og oppbevaringstid blir påvirket av defektenes natur, graden av korreksjon, injeksjonsdybden, legens injeksjonsteknikk og individets fysiske konstitusjon. Overmålig bruk av gel kan føre til risikoen for hevelse, og overdreven korreksjon bør unngås.
•Inflammatorisk reaksjon kan forårsakes av laserbehandling, kjemisk pelling eller noen andre behandlinger som kan føre til hudirritasjon etter eller før injeksjon av gel. Dersom pasienten har mottatt ovennevnte behandling, skal det av en faglig lege vurderes at huden er helt helbredet før injeksjon av gel. Ovennevnte behandling bør mottas etter bekreftelse fra en faglig lege 1 måned etter injeksjon av gel.
•Etter at injeksjonen er fullført, bør injeksjonsstedet ikke utsettes for intens varme (som solbrenning) eller ekstreme kalde miljøer innenfor 7 dager. Pasienten bør unngå å innta irriterende medikamenter eller matvarer. Pasienten bør ikke motta hudpleiebehandlinger som massasje og ansiktshudpleie etter eget skjønn; hvis slike behandlinger er nødvendige, bør pasienten kontakte en faglig lege.
•Utslutningsperioden for L-melkesyreglykol-kopolymermikrosfærene som er inneholdt i gelen er relativt lang. Derfor er det fortsatt risiko for subkutane noder, rødhet og kronisk granulomatøs sykdom (KGS) på injeksjonsstedet selv ved normale injeksjoner, bortsett fra ved feilaktig eller overdreven injeksjon.
•Injeksjon av gelen i kroppen fører sjelden til spredning eller forskyvning av mikrosfærene. Mikrosfærene som er inneholdt i gelen, er vanskelige å fjerne direkte gjennom kirurgisk snitt. Hvis lokal vevsødem, indurering eller KGS oppstår som følge av spredning eller forskyvning av mikrosfærer, kan topisk eller oral kortikosteroidbehandling og lokal antiinflammatorisk behandling administreres. Ved behov kan lesjonene fjernes kirurgisk sammen med mikrosfærene.
•Unntatt ved korreksjon av nasolabiale folder, er produktet ikke egnet til bruk på andre områder ettersom sikkerhet og effekt ikke er dokumentert.
•Bortsett fra de dype lagene av dermis og subkutane overfladiske og dybe lag, er produktet ikke egnet til bruk på andre lag siden sikkerhet og effekt ikke er dokumentert.
•Sikkerheten og effekten ved multiple injeksjoner av gelen er ikke dokumentert.
•Sikkerheten og effekten av gelen hos gravide/ammer, mindreårige og eldre personer over 65 år er ikke dokumentert. Det anbefales at gelen brukes i befolkningen mellom 18–65 år.
•Sikkerheten og effekten av gelen i kombinasjon med andre legemidler og enheter er ikke dokumentert.
•Produktet skal kasseres som medisinsk avfall etter bruk eller etter utløpsdato.
FORVENTET UNGUNSTIGE REAKSJONER
En lokal, kortvarig, injeksjonsrelatert reaksjon kan oppstå etter gelinjeksjon. Mulige reaksjoner omfatter hovedsakelig rødning, blåmerter, smerte, svelling og jukling på injeksjonsområdet. Disse reaksjonene oppstår vanligvis den dagen injeksjonen gjøres eller innen 3–5 dager etter injeksjon, og forbedrer seg vanligvis spontant etter omtrent 1–4 uker. Vanligvis er enkle behandlinger som iskompress tilstrekkelig. Hvis symptomer er alvorlige, anbefales det å kontakte en lege for passende klinisk behandling basert på alvorenheten.
SJÆLDSOMME UNGUNSTIGE REAKSJONER
•Hudavfarging på injeksjonsstedet kan skyldes lidokain som induserer lokal kapillærkonstriksjon.
•Noen pasienter kan utvikle indurasjon eller små knuter ved injeksjonsstedet, som er relatert til injeksjonsteknikken og kan være enten akutt (innen 1 måned etter injeksjon) eller forsinket (flere måneder etter injeksjon). Små knuter løser seg vanligvis spontant. Ved alvorlige knuter kan topisk kortikosteroid benyttes for behandling. Større knuter eller de som er resistente mot medisinering, kan kreve kirurgisk fjerning, noe som bør diskuteres med en lege.
•Noen pasienter kan oppleve allergiske reaksjoner på kort tid, slik som lokal erytem, svak hevelse og kløe. I alvorlige tilfeller kan det føre til lokale papler eller hvieleser. Pasientene kan kontakte en lege for å få behandling med topiske eller orale kortikosteroider i kombinasjon med fysisk behandling som koldkompress. Ved behov kan det utføres immunogenscreening for å forebygge fremtidige allergireaksjoner.
•Noen pasienter kan oppleve infeksjon på implantatstedet på kort eller lang sikt. Rådfør deg med en lege for regulær antibehandling og vurder drenering ved hjelp av snitt hvis nødvendig.
•Noen pasienter kan oppleve akutte eller kroniske alvorlige lokale betennelsesreaksjoner, hudpigmentering osv. Rådfør deg med en lege for antiinflammatorisk og antihistaminbehandling. Etter at den betennelsesaktive fasen er over, kan man vurdere å motta annen relatert behandling for å fjerne pigmentering.
•Det er ikke rapportert noen bivirkninger som granulom, epidermal nekrose og hives i kliniske prøver av produktet; hvis tilstede, kan disse bivirkningene lindres ved å bruke lokalt eller peroralt kortikosteroid i flere uker til måneder. Produktet bør ikke brukes hos pasienter som har opplevd lignende bivirkninger tidligere.
•Den uønskede reaksjonen vaskulær embolisme har ikke blitt rapportert i kliniske prøver av produktet. Hvis gelen ved en feiltakelse blir injisert i et blodkar på grunn av feil operasjon, og pasienten opplever noen av følgende symptomer som forandringer i synet, hvitfarging av huden i det rammede området eller unormal smerte, bør injeksjonen stoppes umiddelbart. Hvis pasienten opplever ovennevnte symptomer etter injeksjon, bør han/hun søke legemiddelbehandling med en gang. Injeksjon av hyaluronidase lokalt kan brukes til å oppløse natriumhyaluronatgelen. For fjerning av mikrosfærer kan en helhetlig terapeutisk tilnærming bli brukt, inkludert fremmelse av vasodilatasjon, behandling av hudskader, ernæring og antiinflammatorisk behandling. Dette kan innebære lokal varmepåske, bruk av vasodilatorer som nitroglyserin, påføring av antibiotika lokalt eller systemisk antibiotikabehandling og bruk av lokale eller orale kortikosteroider til behandling.